Статьи
Есть ли жизнь после иммунотерапии уротелиального рака?
Новые иммунопрепараты постепенно входят в практику онкологов и присутствуют в Перечне жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП) на 2018 год. Все более актуальным становится вопрос и о последующем лечении при прогрессировании после иммунотерапии. Результаты нескольких исследований показывают возможность эффективного лечения данной категории пациентов.
ИММУНОТЕРАПИЯ — УЖЕ В ЖНВЛП-2018
Сразу 5 иммуноонкологических препаратов включены в американские клинические рекомендации по лечению метастатического рака мочевого пузыря (мРМП): атезолизумаб, пембролизумаб, ниволумаб, дурвалумаб и авелумаб. Все они относятся к анти-PD-1 или анти-PD-L1 антителам и присутствуют в аналогичных европейских рекомендациях, за исключением дурвалумаба и авелумаба, так как эффективность последних подтверждена только данными клинических исследований (КИ) I/II и Ib фазы (низкая доказательность).
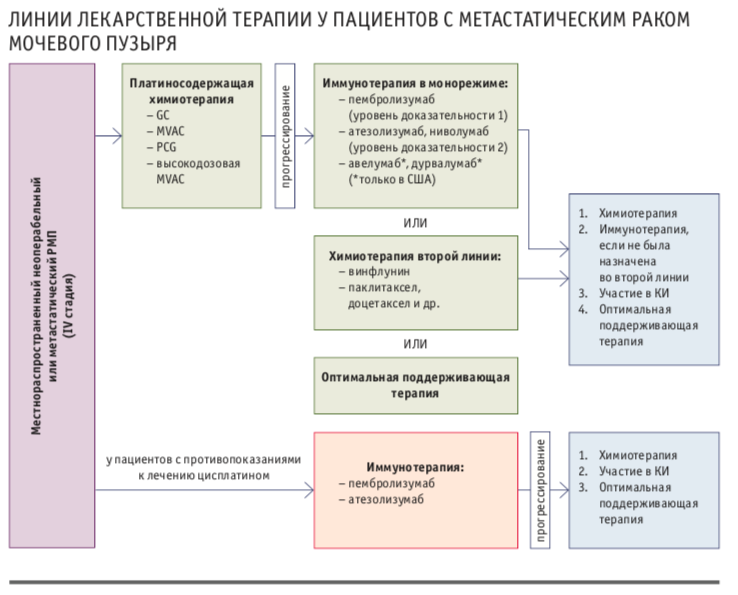
Атезолизумаб и пембролизумаб одобрены FDA и Европейским агентством лекарственных средств (EMA) для применения в первой линии у больных местнораспространенным неоперабельным и метастатическим РМП, которые не могут перенести лечение цисплатином. Известно, что почти у каждого второго пациента есть какие-либо противопоказания к назначению цисплатинсодержащих комбинаций.
Для второй линии при прогрессировании мРМП после платиносодержащей химиотерапии одобрены атезолизумаб и ниволумаб (на основании результатов КИ II фазы) и с наивысшим, 1 уровнем доказательности — пембролизумаб (КИ III фазы). Этот препарат показал достоверное увеличениеобщей выживаемости пациентов по сравнению со всеми опциями химиотерапии второй линии (паклитаксел, доцетаксел и винфлунин).
Новые показания для иммунотерапии были одобрены и Минздравом РФ. Ряд препаратов (пембролизумаб, ниволумаб) были включены в Перечень жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП) на 2018 год.
Очевидно, уже в ближайшем времени следует ожидать расширения назначения иммунотерапии у больных мРМП, которым невозможно проведение стандартной платиносодержащей химиотерапии, а также при подтверждении прогрессирования на фоне или после ее применения.
ТРЕТЬЯ ЛИНИЯ БЕЗ ЧЕТКИХ РЕКОМЕНДАЦИЙ
Важным преимуществом иммунотерапии является возможность достижения длительной ремиссии заболевания. Но пока не решено, стоит ли прекращать иммунотерапию после подтверждения полного рентгенологического ответа? Кроме того, можно ли повторно возвращаться к иммунотерапии анти-PD-L1/анти-PD-1?
При этом узначительной доли пациентов наблюдается ограниченная эффективность иммунотерапии. Так, в первой линии частота объективного ответа (ЧОО) на пембролизумаб или атезолизумаб достигает 29 %, полных ответов, соответственно, 7 % и 9 %. Во второй линии (после химиотерапии) эффективность снижается:
ЧОО на ниволумаб — только 19,6 %, на атезолизумаб— 15 % и чуть выше (21,6 %) — на пембролизумаб. Прослеживается четкая закономерность повышения ЧОО до 23,8 % у пациентов с высокой степенью экспрессии PD-L1 в опухоли (≥1 %) и еще существеннее (28,4 %) — при гиперэкспрессии PD-L1 (≥5 %).
И все-таки, в сравнении с иммунотерапией, химиотерапия второй линии показывает существенно меньший противоопухолевый ответ — 11,4 % (достоверное различие с пембролизумабом, P=0,001, по данным исследования KEYNOTE-045). Кроме того, наблюдается краткосрочная длительность объективного ответа на химиотерапию по сравнению с иммунотерапией.
Четких рекомендаций по лечению после иммунотерапии на сегодняшний день не существует. Европейские практические руководства (EAU) допускают возможность назначения в третьей линии монохимиотерапии винфлунина.
Согласно американским рекомендациям NCCN, пациентам после предшествующей иммунотерапии должно быть предложено участие в клинических исследованиях или (при отсутствии такой возможности) возможность назначения различных режимов химиотерапии, в зависимости от наличия противопоказаний к цисплатину: режим GC, монотерапия гемцитабином, монотерапия карбоплатином, nab-паклитакселом, доцетакселом, пеметрекседом и другие режимы. К настоящему времени каких-либо рандомизированных исследований в этой области не проводилось.
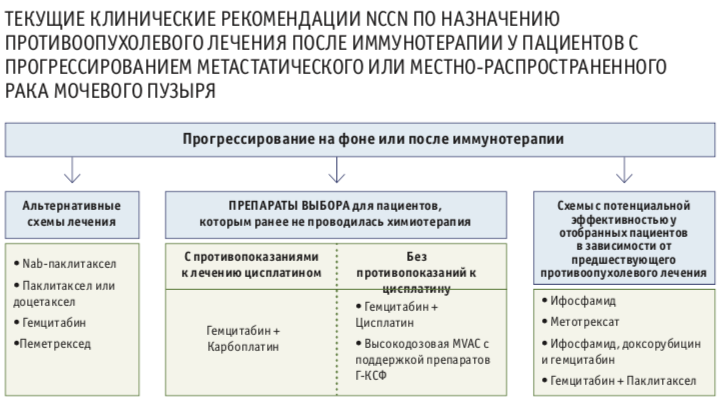
FDA ОБОЗНАЧИЛО ПРОРЫВ В ТЕРАПИИ
В марте 2018 года FDA признало «прорывом в терапии» (Breakthrough Therapy Designation) применение нового рекомбинантного препарата энфортумабаведотина для лечения больных местнораспространенным неоперабельным или метастатическим РМП, которым ранее проводилась иммунотерапия ингибиторами иммунных контрольных точек (анти-PD-L1/анти PD-1 препаратами). Энфортумабведотин представляет собой рекомбинантный препарат —конъюгат моноклонального антитела (анти-Нектин-4) и цитотоксического препарата (монометилауристатин Е), действующего на внутриклеточный аппарат микротрубочек.
На решение FDA повлияли результаты клинического исследования I фазы, в котором участвовали пациенты с метастатическими солидными опухолями, в том числе и больные мРМП. Средний возраст участников исследования составил 67 лет (диапазон 41–84).
Пациенты получали монотерапию энфортумабом ведотином в различных дозах (0,5; 0,75; 1 и 1,25 мг/кг массы тела внутривенно) каждые 3 из 4 недель до прогрессирования или появления непереносимой токсичности. У 85 % пациентов была предшествующая платиносодержащая химиотерапия, у 46 % — иммунотерапия, у 43 % — химиотерапия таксанами. Экспрессия нектина-4 обнаружена у большинства (87 %) пациентов.
В когорте больных мРМП (n=71) объективный ответ на терапию энфортумабом ведотином был достигнут у 41 % пациентов (95 % ДИ 29,3–53,2), и у 4 % наступила полная регрессия опухоли. При анализе объективного ответа на препарат в дозе, рекомендуемой для II фазы исследования (n=30 пациентов), ЧОО составила 53 % (95 % ДИ 34,3–71,7), полный ответ — у 1 пациента (3 %) и стабилизация заболевания —у 18 %. При подгрупповом анализе только тех пациентов, которые получали ранее иммунотерапию, ЧОО составила 47 % (n=8), стабилизация заболевания наступила у 5 пациентов. К моменту завершения наблюдения лечение продолжали получать 26 % пациентов. Медиана длительности лечения составила 15,1 недели (диапазон 1,1–64,6). Проявлениями токсичности 3–4 степени были мочевая инфекция (8 %), гипофосфатемия (3 %), гипонатриемия (5 %), анемия (8 %) и гиперурикемия (5 %).
Изучение эффективности и безопасности препарата продолжено в рамках КИ II фазы EV-201 (монотерапия 120 пациентов с мРМП, получавших иммунотерапию) и Ib фазы EV-103 (комбинация энфортумаба ведотина с пембролизумабом или атезолизумабом).
ХИМИОТЕРАПИЯ ЭФФЕКТИВНА ПОСЛЕ ИММУНОТЕРАПИИ
Первый опыт применения химиотерапии после предшествующей иммунотерапии у больных мРМП опубликовали в феврале 2018 г. Совместная работа ученых из Великобритании и Нидерландов была отмечена редакцией журнала European Urology в номинации Platinum Priority.
Обязательным условием включения пациентов в исследование стало наличие подтвержденного по критериям irRECIST прогрессирования после иммунотерапии анти-PD-L1/анти-PD-1 препаратами. Иммунотерапия проводилась в первой линии (группа А) или после платиносодержащей химиотерапии (группа В). В обеих группах 86 % пациентов имели висцеральные метастазы. Медиана наблюдения составила 8,2 мес (6,5–11,3).
Полных регрессий опухоли в исследовании не было. Среди пациентов, уже получавших химиотерапию первой линии и иммунотерапию, противоопухолевый ответ на химиотерапию в третьей линии был достигнут у 3 (21 %), стабилизация процесса — у 10 (71 %) пациентов. Важно отметить, что проводилась преимущественно ХТ карбоплатином и паклитакселом (50 %) или доцетакселом (21 %). Платиносодержащие режимы GC и гемцитабин+карбоплатин смогли получить, соответственно, только 7 % и 21 % пациентов. Ожидаемо лучшие результаты получены при проведении химиотерапии во второй линии после иммунотерапии: частота объективного ответа — 64 %, стабилизация заболевания — 21 %. В этой группе пациенты получали только стандартную платиносодержащую ХТ (в т. ч. GC — 29 %).
Исследование показало, что проведение иммунотерапии после первой линии химиотерапии не ухудшает результаты последующей химиотерапии. Вероятно, не существует перекрестной резистентности между иммуноонкологическими и цитотоксическими препаратами. В то же время нет достаточных данных, позволяющих утверждать о потенцировании и аддитивном эффекте иммунотерапии и последующей химиотерапии.
В дальнейшем результаты проспективных рандомизированных исследований позволят определить, будет ли оптимальным назначение последовательной (химиотерапия → → иммунотерапия → химиотерапия) или комбинированной иммунохимиотерапии.
Список литературы находится в редакции.

















